Date: February 2021
Successful treatment of breast cancer by immunotherapy continues to be a challenge, but emerging clinical data is encouraging.3 To help enable preclinical research of immunotherapy in breast cancer, we have developed the orthotopic EMT6 syngeneic breast tumor model in 2018.
The EMT6 model was derived from a transplanted hyperplastic alveolar metastatic lung nodule in BALB/c mice.4 As further data was generated with this model, observations of metastatic foci in the lung visible upon gross necropsy occurred in up to 40% of control mice. As metastasis is common in breast cancer patients, it was important to take advantage of this finding, so a luciferase enabled EMT6 cell line (EMT6-Luc) was generated to monitor thoracic metastasis by bioluminescence imaging (BLI) in vivo. For this project, animal care and use was conducted according to animal welfare regulations in an AAALAC-accredited facility with IACUC protocol review and approval.
このスポットライトでは、EMT-6-Luc モデルの初期有効性研究から得られたデータを紹介します。同モデルは乳房脂肪体(MFP)に移植され、キャリパー測定による原発腫瘍の測定および胸部の BLI 観察の両方により転移進行の監視が行われました。図 1 は EMT6 および EMT6-Luc モデルにおける対照腫瘍の増殖を示しています。親モデルと EMT6-Luc モデルの両方で、MFP 腫瘍の平均倍加期間は 5.5 日間であり、試験薬の抗腫瘍活性を評価する期間として、治療濃度域である 2~3 週間を見込めることが分かります。

図 1。メスの Balb/c マウスに同所移植(乳房脂肪体)された EMT6(A)および EMT6-Luc(B)の増殖がそれぞれ抑制されていることを示す。
MT6-Luc のチェックポイント阻害剤への反応を判定するため、EMT6-Luc を移植されたマウスを抗 mPD-1 または抗 mPD-L1 によって治療しました。その結果、チェックポイント阻害剤への反応は対照に比べると穏やかであり(図 2)、EMT6-Luc における抗 mPD-1 への反応は、親系統から得られた同様のデータと類似していることが分かりました(表 1)。抗 mPD-L1 に対する EMT6-Luc の反応は、親系統に比べてわずかに増加しているように見て取れます(表 1)。しかし、試験条件下の抗腫瘍効果に関しては、ルシフェラーゼ群の追加が全体にもたらす影響は最小限であると言えます。
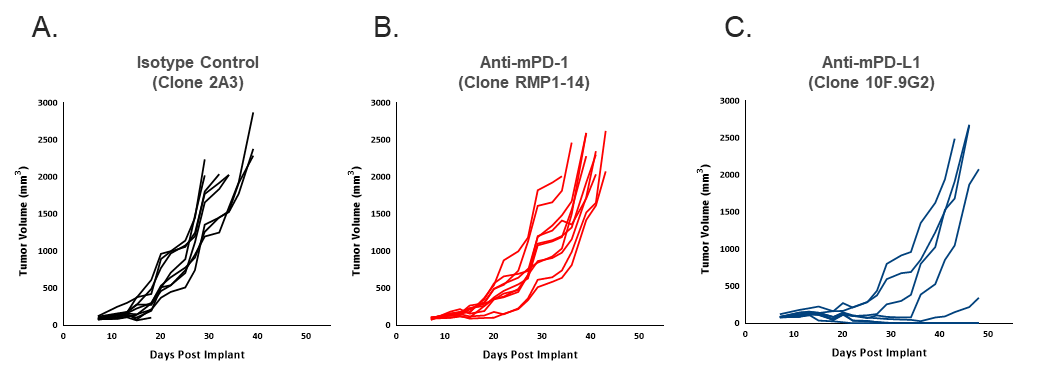
図 2。EMT6-Luc 腫瘍の体積測定結果が、アイソタイプコントロール(A)と比較した際の、抗 mPD-1(B)および抗 mPD-L1(C)の抗腫瘍効果を示している。各抗体は週に 2 度、10 mg/kg を投与。
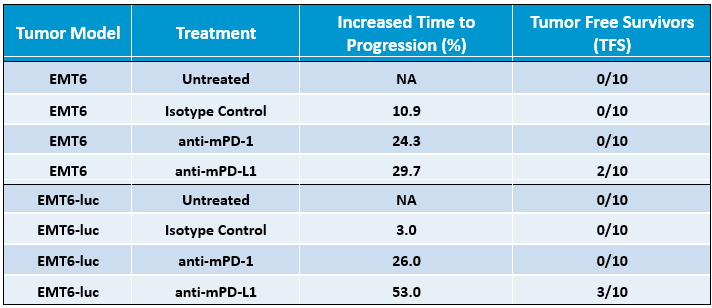
表 1。抗 mPD-1 と抗 mPD-L1 によるチェックポイント阻害への反応を利用し、EMT6 および EMT6-Luc 腫瘍モデルの反応差を示している。無増悪期間項目の増加は、未治療の腫瘍と比較した際の治療開始から動物実験を終える日までの日数の増加に基づきます。
MFP の原発腫瘍の測定を用いて治療に対する反応を評価する方法に加え、ルシフェラーゼ発現細胞株を使用することで、BLI 信号の位置から胸部の転移進行を in vivo で監視することも可能になります。図 3 は胸部の信号の増加を示します。予想した通り、BLI を用いた監視により、転移が起こる範囲だけでなく、抗 mPD-1 や 抗mPD-L1 による治療がもたらす転移の遅れを、より高い精度で確認することができました。この実験ではすべての対照動物において胸部の BLI 信号の増加が見られましたが、肉眼剖検で転移性結節が確認されたものはありませんでした(表示データなし)。胸部の信号が増加した原因を確定するにあたり、病理学的評価は必要となりますが、未治療の動物の解剖による肺結節の経時的な観察結果から考察すると、信号の増加は転移が原因であり、今回の評価項目の重要性を強調する結果となりました。この仮定に基づくと、抗 mPD-L1 を用いた治療により、転移の開始時期に遅れが生じるとともに原発腫瘍の増殖も遅くなると結論付けることができます。さらに注目すべきは、このモデルの転移が健康の悪化を引き起こすわけではない点です。マウスは転移の進行による健康への影響が出る前に、原発腫瘍組織量が原因で実験を終えています。
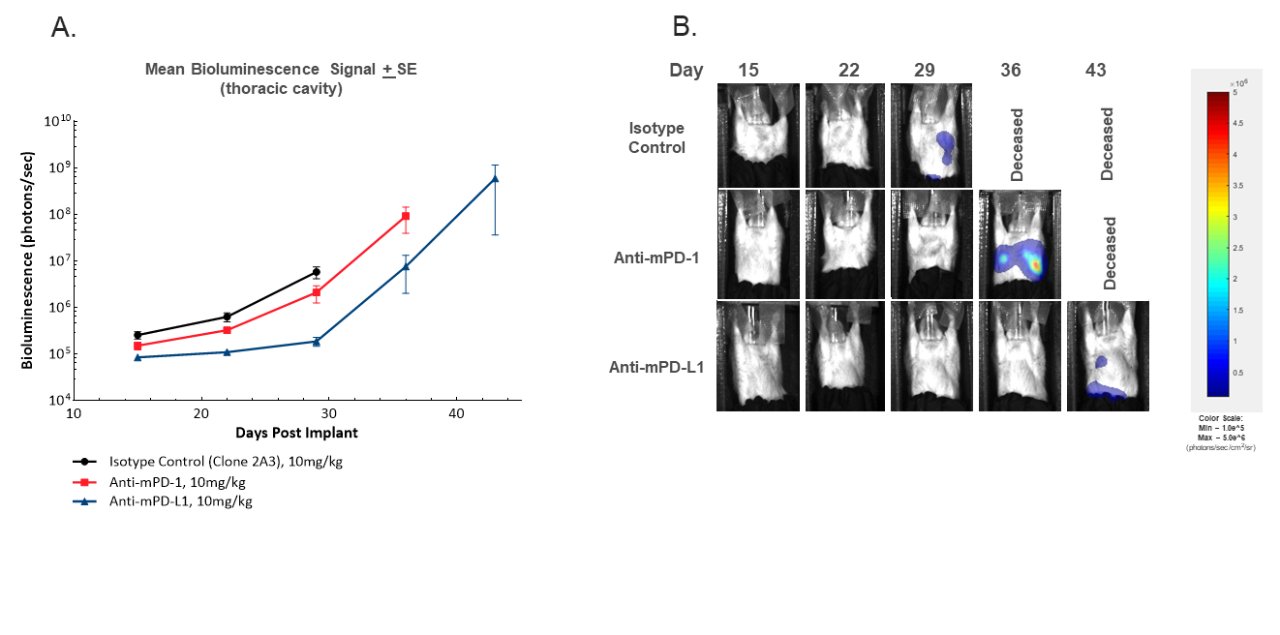
図 3。In vivo での BLI 画像化を用いて時間の経過とともに胸部の信号が増加する過程を監視。胸部の平均腫瘍組織量(A)または典型的な BLI 画像化(B)。
Immuno-Oncology の目的でモデルを研究する際には、腫瘍内の浸潤細胞の組成を知ることも重要です。このため、150~550mm3の未投薬腫瘍について、全 CD45+ 細胞の割合を表す T 細胞および骨髄性細胞の浸潤の有無を調べました(図 4)。すべての腫瘍の骨髄コンパートメントは、M2 マクロファージ、単球性 MDSC、および顆粒球 MDSC に均等に配分されています。M1 マイクロファージ浸潤は、他の骨髄由来細胞に比べて比較的低く、また、EMT6 腫瘍と比べると EMT6-Luc 腫瘍内で少し高いという結果になりました。また、CD4+ および CD8+ T 細胞の浸潤は最小限であり、この結果は、EMT6 および EMT6-Luc 腫瘍でも同様となりました。ただし、EMT6-Luc 腫瘍内の NK 細胞にわずかな増加が確認されました。この組成は、免疫抑制性の微環境を示唆しており、試験を行った免疫療法の反応が限定的であったことを説明するうえで役に立つ可能性があります。
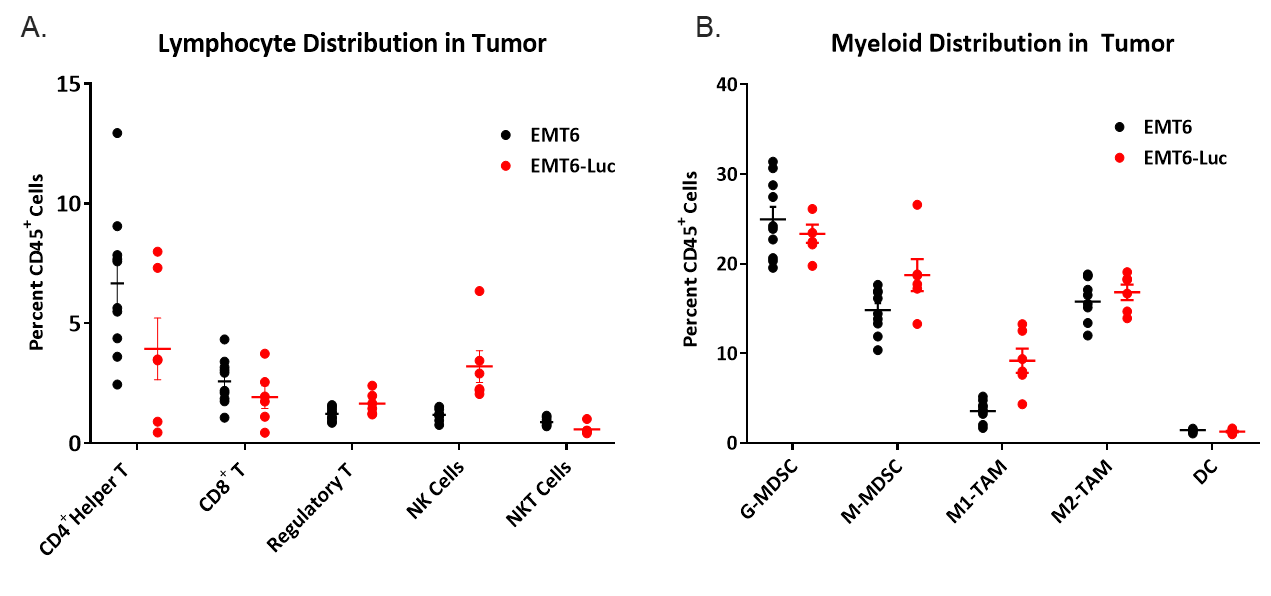
図 4。ナイーブ EMT6 および EMT6-Luc 腫瘍内におけるリンパ系免疫細胞(A)および骨髄性免疫細胞(B)の分布を示す。
EMT6-Luc マウス乳癌モデルは、マウスの完全な免疫系を使用し、Immuno-Oncology において強力なツールとなる有益な免疫プロファイルを持っています。これらのデータは、EMT6-Luc モデルが安定した前臨床の Immuno-Oncology モデルであることを裏付け、同モデルは原発腫瘍の成長や乳癌の遠隔転移の様子を評価する場合に有益と言えます。
Please contact us to speak with our scientists about how EMT6-Luc, or one of our other syngeneic models, can be used for your next immuno-oncology study.
参照
1「米国癌協会:Cancer Facts & Statistics」 米国癌協会 | Cancer Facts & Statistics、cancerstatisticscenter.cancer.org/?_ga=2.5394928.293340281.1606765768-996476487.1605734560.
2 Howlader N, Noone AM, Krapcho M, Miller D, Brest A, Yu M, Ruhl J, Tatalovich Z, Mariotto A, Lewis DR, Chen HS, Feuer EJ, Cronin KA (eds). SEER Cancer Statistics Review、1975-2017、米国がん研究所(National Cancer Institute)。Bethesda 医師、https://seer.cancer.gov/csr/1975_2017/、監視疫学遠隔成績プログラム(SEER)ウェブサイトに2020年4月に掲載された、2019年11月提出データに基づく。
3Leal JHS and McArthur H. Breast cancer immunotherapy: From biology to current clinical applications. Eur. Med. J., 2020; 5(2): 113-124.
4Rockwell SC, Kallman, RF, Fajardo, LF. Characteristics of a Serially Transplanted Mouse Mammary Tumor and Its Tissue-Culture-Adapted Derivative. J. Natl. Can. Inst., 1972; 49(3): 735–749.
お問い合わせはこちら
お問い合わせ