著者:Dylan Daniel 博士 - サイエンティフィック・ディベロップメント部門ディレクター
Date: November 2017
ID8-Luc は、同所性卵巣癌の治療を目的に開発された新しい同種マウスモデルです。卵巣癌は、かなり進行の進んだステージ 4 と診断された患者の 5 年の生存率が 17% であり、医療発達の重大な必要性を残しています。
卵巣癌は、未だ医療ニーズの満たされていない領域であり、かなり進行した状態で見つかることが多いことから致死的な疾患となっています。米国では2017年に約 22,440 人の女性が新たに卵巣癌と診断され、死者は 14,080 人になると推定されています。米国における標準治療は、プラチナとタキサン系抗有糸分裂剤を併用した化学療法ですが、こうした治療は通常、最初はうまくいくものの、やがて再発が生じ病勢が進行します。したがって、卵巣癌の新しい治療アプローチが求められているわけです。
最近は、その他の癌を治療するための免疫系強化の取り組みが成功していることから、卵巣癌でも免疫療法の創薬の試みが行われるようになりました。現在、免疫療法の治療薬とその併用を検証する治験が 50 件以上進行しています。しかし、前臨床薬理試験に使用できる同系マウス卵巣癌モデルの数が限られているのも事実です。 Labcorp has developed the ID8 syngeneic mouse cell line model for testing standard therapeutics as well as for immuno-oncology applications.ID8 は、C57BL/6 マウス卵巣癌の表面上皮細胞を In vitro で連続継代して形質転換させたもので 1、 ID8 細胞(ID8-Luc-mCherry-Puro)にルシフェラーゼを発現させており、同所性(腹腔内)移植したあと腫瘍の増殖を生物発光イメージング(BLI)でモニタリングできるようになっています。
図 1A と図 1B はそれぞれ ID8-Luc-mCh-Puro の腫瘍増殖動態を BLI でモニタリングした時の全体平均とグループ別のデータです。細胞を C57BL/6 アルビノマウス 1 匹あたり 5.0×106 個移植したグループと 1.0×107 個移植したグループとでは、後者でより一貫した増殖が認められました。シグナル(光子数 / 秒)は予想通り、腫瘍細胞の発光を吸収する皮膚のメラニン色素が欠乏している C57BL/6 アビルノマウス(緑色の線、図 1B 、グループ 2)が野生型 C57BL/6 マウス(赤い線、図 1B)よりも高くなっていました。図 1C は、ID8-Luc-mCh-Puro 同所モデルの病勢の進行を捉えた典型的な BLI 画像です。
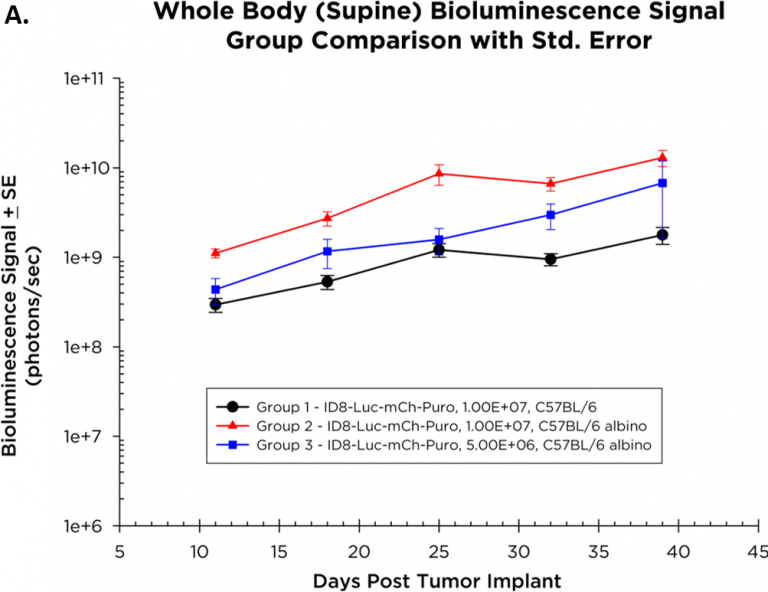
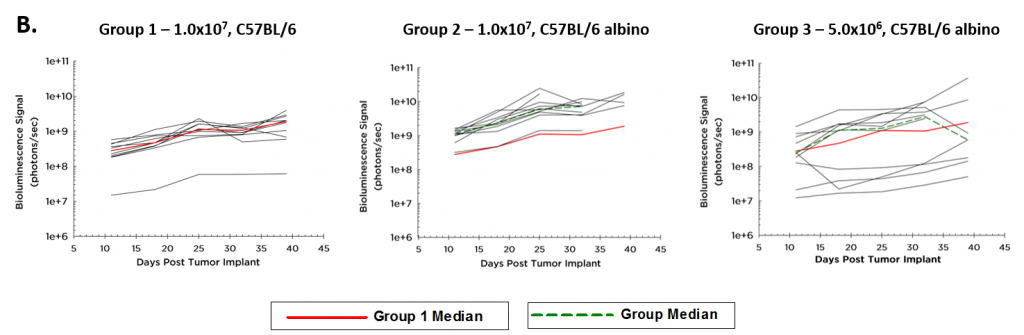
Fig. 1B – Growth Kinetics of Tumor-ID8-Luc-mCh-Puro
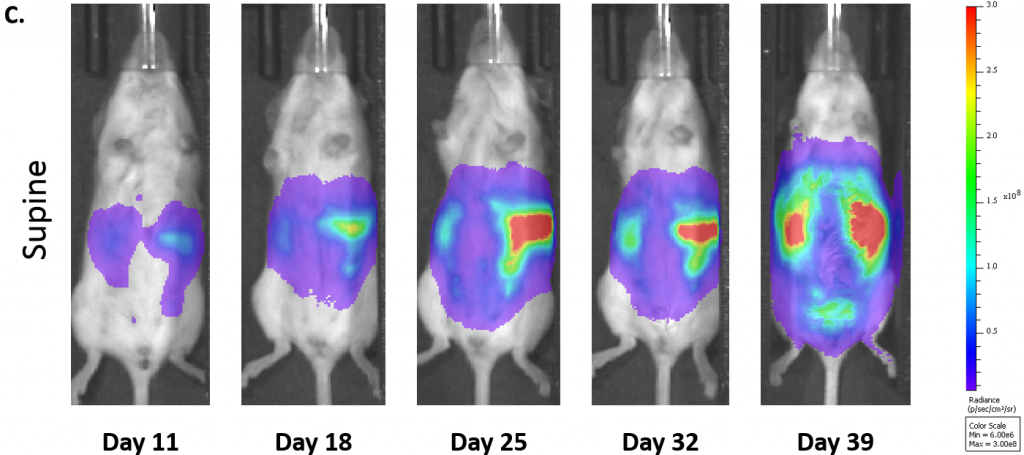
図 1C:ID8-luc-mCh-Puro を C57BL/6 アルビノマウスに移植(細胞数 1.0×107 個 / 1 匹)した後の卵巣癌進行を捉えた典型的 BLI 画像
試験中、ID8-Luc-mCh-Puro 細胞を移植したマウスの体重は増加し(図 2)、減少については一部で終盤にのみ見られました。1.0×107 個の細胞を移植した C57BL/6 アルビノマウスでは、腹水の貯留による腹部膨満が現れ、病勢は直線的に進行(図 3)、生存期間は 35〜40 日でした。
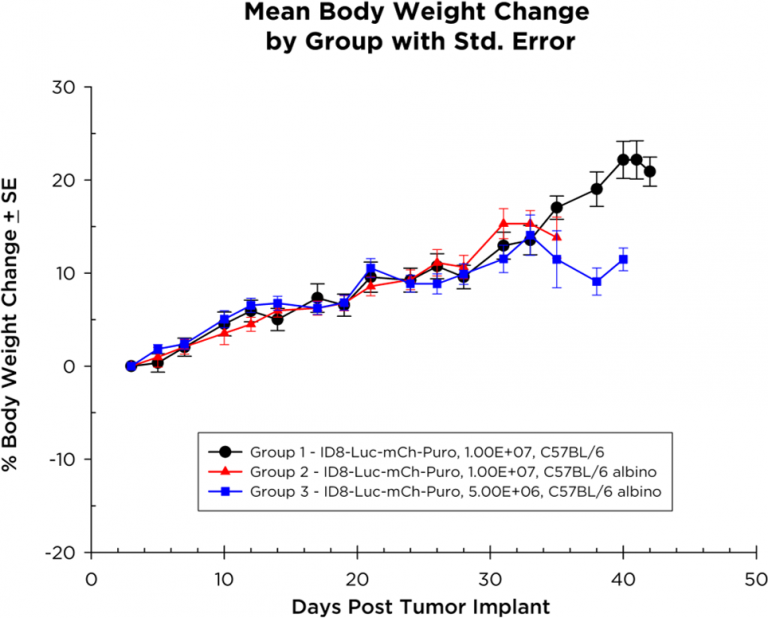
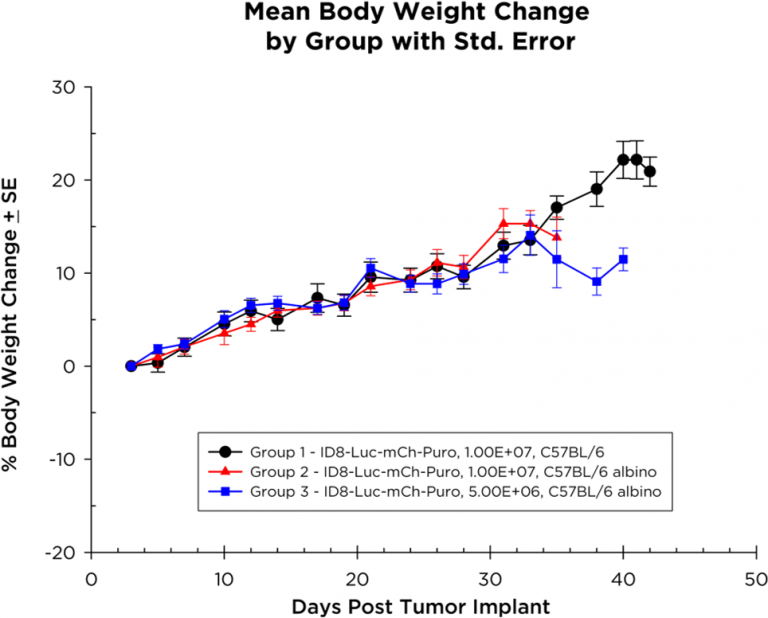
図 3:同所性 ID8-luc-mCh-Puro 卵巣癌を持つマウスの生存動態
Labcorp performed immune profiling of the ascites from the ID8-Luc-mCh-Puro bearing mice. In Table 1, the immune profiles for total CD45+ leukocytes, CD4+ T cells, CD8+ T cells, Tregs, M-MDSC, G-MDSC, M1 TAM and M2 TAM are shown. While there is considerable heterogeneity in the immune profile between mice, all mice have a robust CD8+ T cell infiltration with favorable CD8+ T cell/Treg ratios. The ID8 ovarian cancer model has been reported to respond to IL-12 immunotherapy which combined with the favorable CD8+ T cell/Treg ratio suggests that the model should support testing of novel immunotherapies.2 Studies to analyze response to immunotherapies as well as standard of care are currently under development.
表 1:ID8-Luc-mCh-Puro 卵巣癌マウス腹水中免疫細胞サブセットのフローサイトメトリーによる個体別プロファイリング
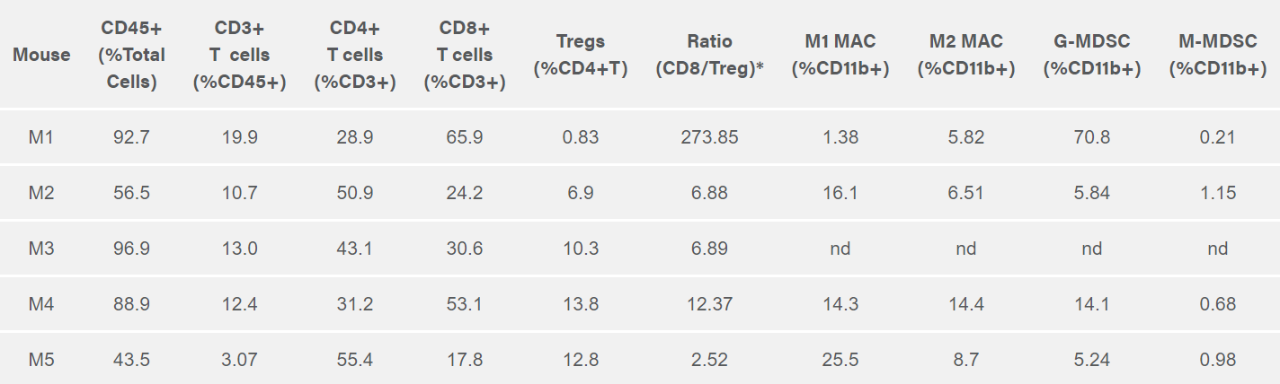
表 1:ID8-Luc-mCh-Puro 卵巣癌マウス腹水中免疫細胞サブセットのフローサイトメトリーによる個体別プロファイリング
*CD8 / Treg 比は、ゲーティング後の CD8、Treg それぞれの絶対数で決まります。
nd = 未決定
参照
お問い合わせはこちら
お問い合わせ