Date: May 2017
2017年には、多発性骨髄腫の新規症例数は約 30,000 件、そしてそれによる死亡者は 13,000 人近くになると予想されています。しかし、多発性骨髄腫は比較的まれな種類の癌で、生涯リスクは 143 人に 1 人(0.7%)です。多発性骨髄腫と診断されるリスクは年齢とともに上昇し、多くは 65 歳以上です。女性よりもわずかに男性の方が発症率が高く、アフリカ系アメリカ人では発症する可能性が他の人種より約 2 倍高くなっています。けれども、多発性骨髄腫と診断される最大のリスク要因は、その時点ですでに形質細胞疾患を患っているという点です。意義不明の単クローン性高免疫グロブリン血症(MGUS)または孤立性形質細胞腫の患者様は、やがて多発性骨髄腫を発症します。
多発性骨髄腫は、骨髄内で最終分化し、抗体を産生する形質細胞の蓄積を特徴とする B 細胞クローン悪性腫瘍です。骨髄腫細胞内の突然変異、そして様々なサイトカインや成長因子との関わりにより、侵襲性と薬剤耐性が高く、 ほとんどの場合、患者様は病気の最終段階まで無症状です。また、骨(特に脊椎)に局在する傾向にあります。 現在の治療法としては、ドキソルビシンとデキサメタゾンをボルテゾミブと併用する方法が一般的で、 ボルテゾミブを使用すると全奏効率が約 50% にまで上昇します。1
MM.1S は、多発性骨髄腫の新規治療法を評価する細胞株として広く使用されています。MM.1S は 42 歳のアフリカ系アメリカ人女性に由来し、CD25、CD38、CD52、CD59 を発現することが記録されています。 It also expresses the glucocorticoid receptor and is dexamethasone sensitive.2 In an effort to more effectively monitor in vivo disease progression, we transfected the MM.1S line with luciferase (MM.1S-pMMP-LucNeo). 生物発光イメージング(BLI)を使用することで、播種性疾患の経時的な進行状態を観察し、マウスにおける再現性のある In vivo 増殖を発見することができます(図 1 および 2)。
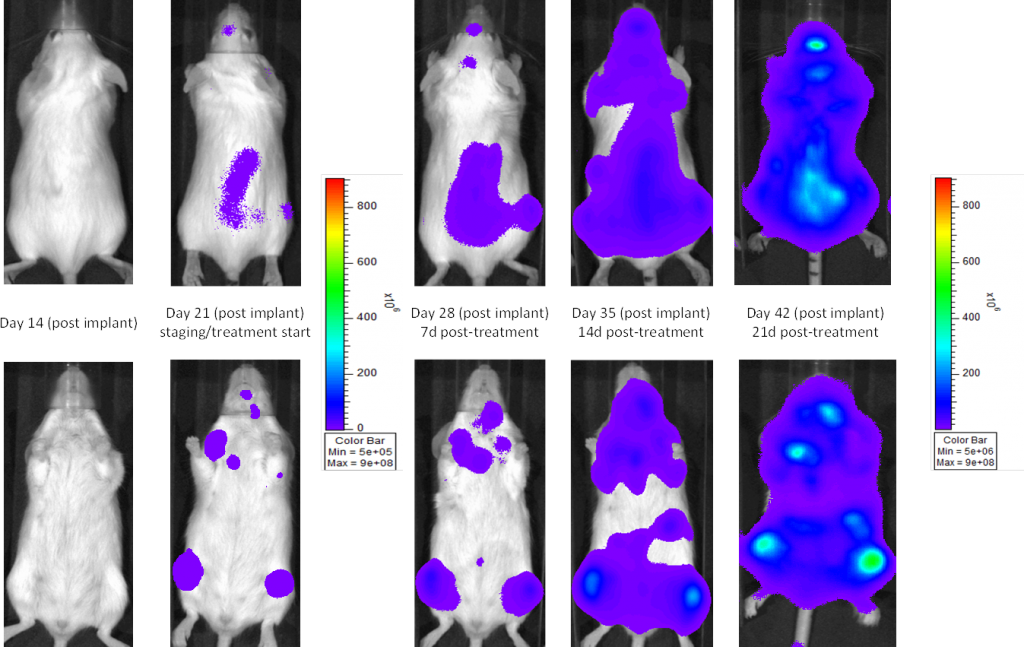
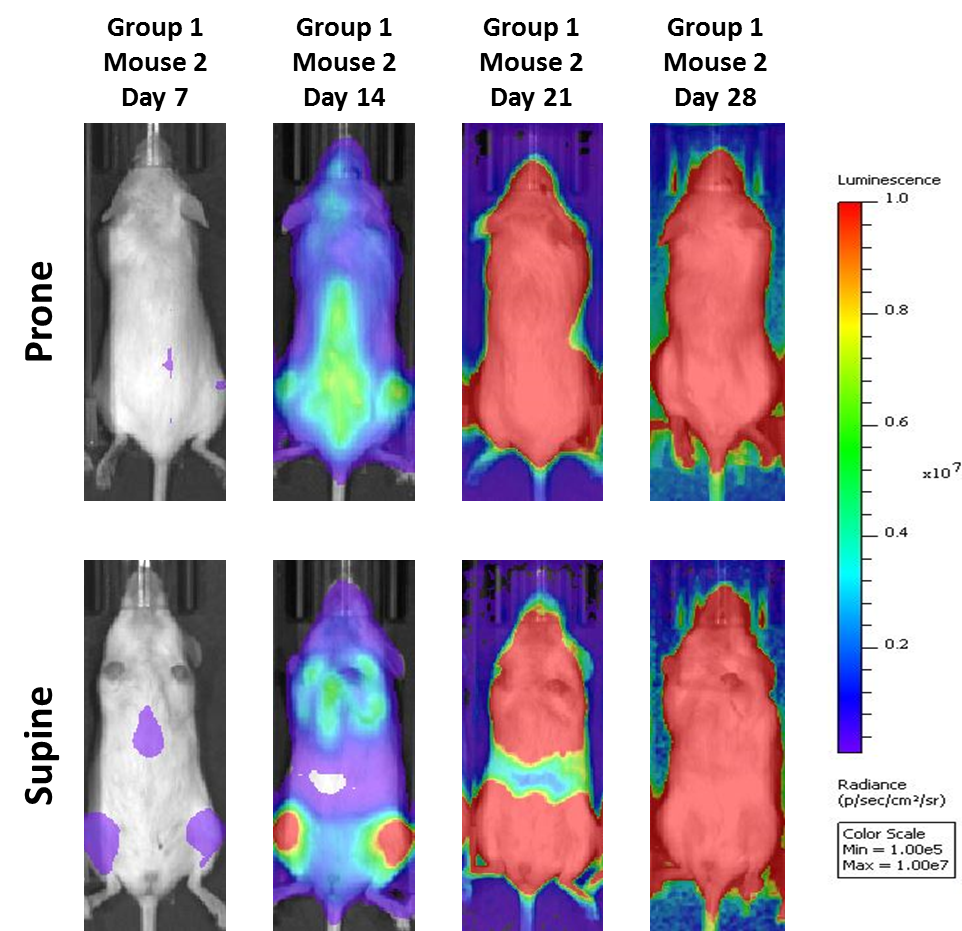
図 2:NSG マウスにおける MM.1S-pMMP-LucNeo ヒト多発性骨髄腫:疾患の進行を示す典型的な画像 - 対照群
総腫瘍量の平均 BLI シグナル
SCID ベージュマウスでは、平均腫瘍量倍加時間は ~2 日(図 3)、死亡率 / 罹患率エンドポイントに達するまでの平均時間は 35-45 日です。MM.1S-pMMP-LucNeo モデルをさらに最適化するため、より侵襲性の高い疾患発症を示す NSG マウス株での増殖の特性を明らかにしました(SCID マウスにおける移植後 7 日と 15 日との比較)。NSG マウスでは、腫瘍量倍加時間は ~1.8 日(図 4)、エンドポイントに達するまでの平均時間は ~21 日で、これは SCID ベージュマウスで観察された全生存期間の約半分でした。
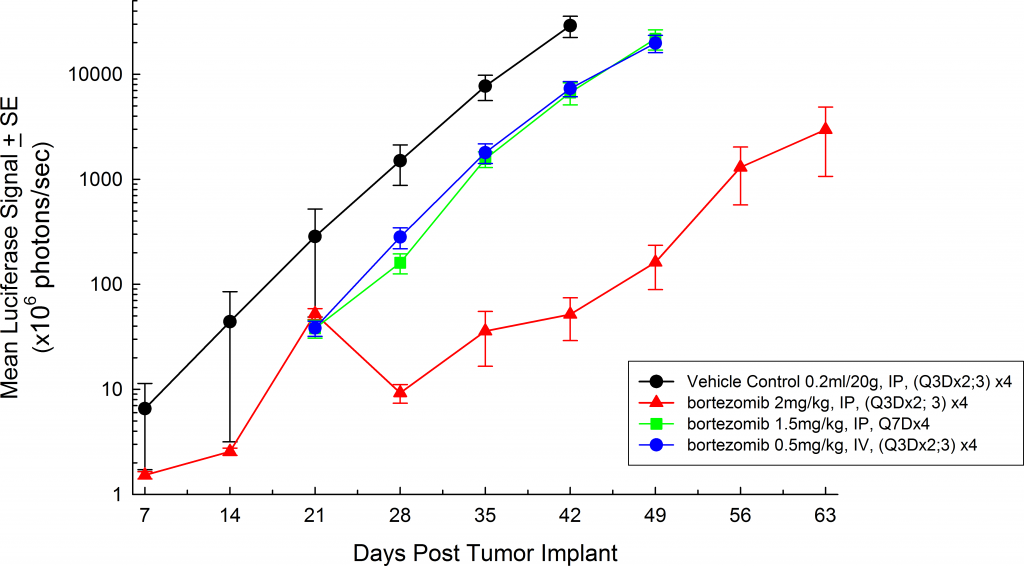
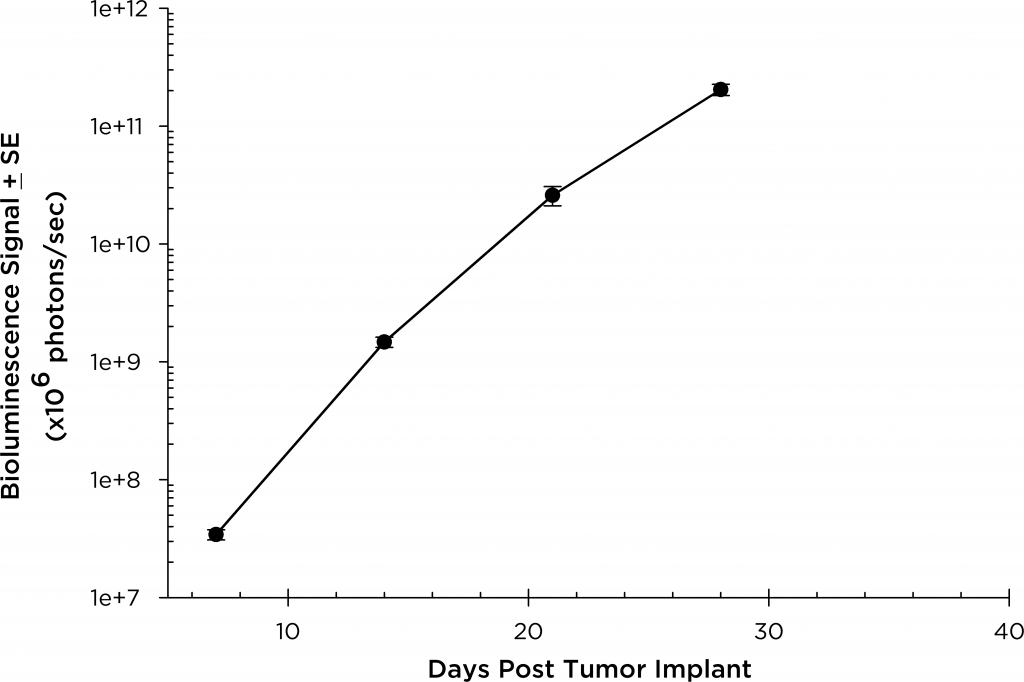
図 3:SCID ベージュマウスにおける MM.1S-pMMP-LucNeo ヒト多発性骨髄腫:総腫瘍量の平均 BLI シグナル
図 4:NSG マウスにおける MM.1S-pMMP-LucNeo ヒト多発性骨髄腫:総腫瘍量の平均 BLI シグナル
体重変化の平均 %
調査したすべてのマウス株において、被検動物は研究期間を通じて比較的無症状であり、疾患の後期段階まで症状を示しませんでした(図 5 および 6)。これは、ヒトにおける症状の現れ方に似ています。マウスにおける一般的な後期の臨床症状としては嗜眠や麻痺が挙げられます。これらの動物の BLI では、脊椎、長骨、下顎骨においてシグナルの局在が見られました。このモデルの疾患進行に対するボルテゾミブ単剤(Velcade®)の効果は限定的でした。このことは、ボルテゾミブを他の薬剤と併用投与した場合に治療に対する反応が改善されることを示す、診療所でのデータに類似しています。MM.1S モデルは、その再現性や、疾患の進行と反応に関するトランスレーショナルな側面を考えると、新しい単剤治療や合剤の評価プラットフォームとして利用できるでしょう。
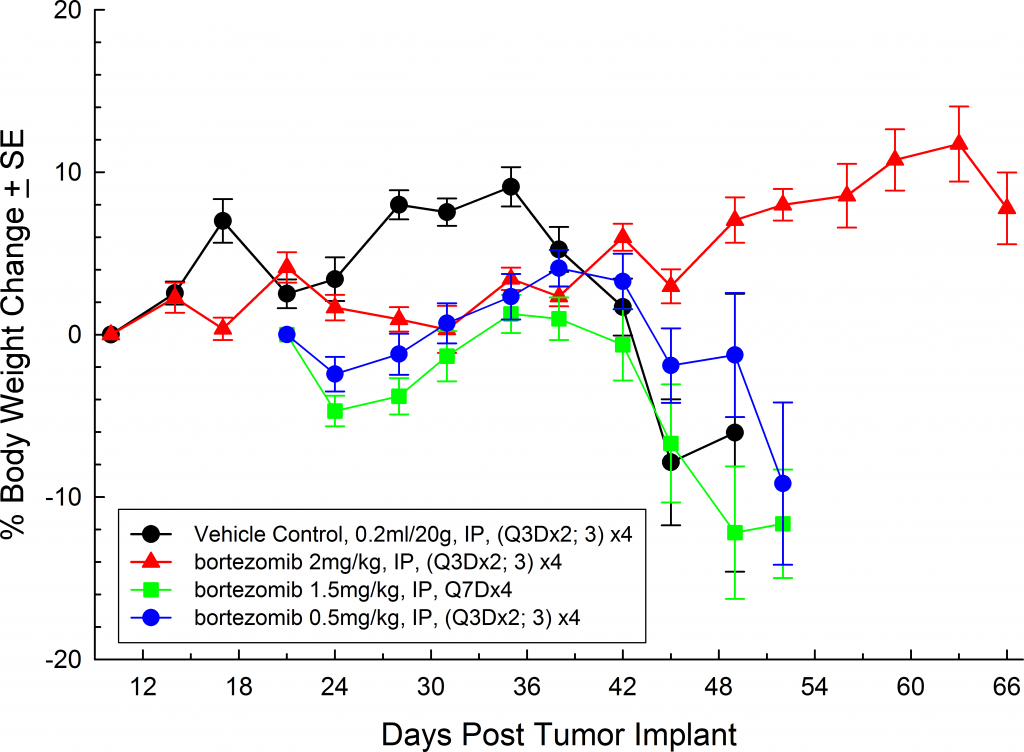
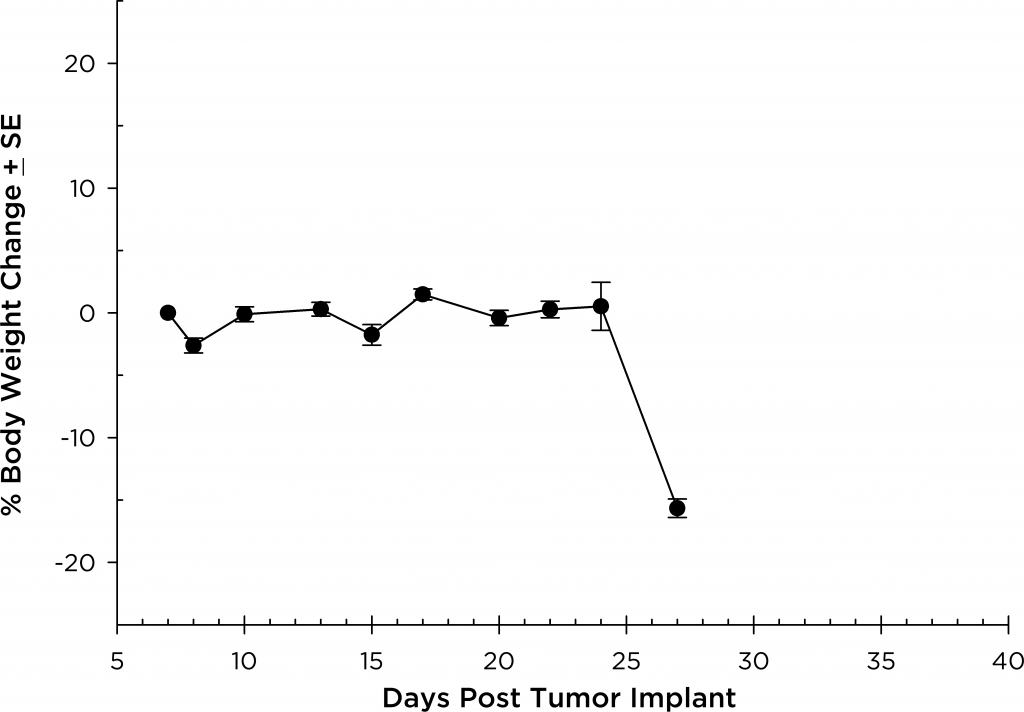
Fig. 5: MM.1S-pMMP-LucNeo human multiple myeloma in SCID Beige mice: Mean % Body Weight ChangeFig. 6: MM.1S-pMMP-LucNeo human multiple myeloma in NSG mice: Mean % Body Weight Change
参照
お問い合わせはこちら
お問い合わせ